
题按:在上一篇短文中,TiPLab磨杵君着重讨论了功能性限定权利要求的支持问题。一般通过缩小权利要求请求保护的范围来克服不支持的缺陷,那么能不能不通过缩小范围来克服呢?请看本篇短文。
该系列文章:
洞见
专利保护抗体发明的挑战和策略(五) 之支持
by
TiPLab磨杵小分队
TiPLab磨杵君通过专利申请实践发现,为了更好地在实质审查过程或者后续的法律程序中争辩权利要求得到了支持,在说明书留有相关的记载,并且在答辩过程中据理力争,也是除了缩小请求保护的范围以外的克服支持问题的一个好方法。让我们来看下一个故事。
▼
第七个故事 亚力史剑桥公司VS 专利复审委员会
TiPLab磨杵君这次要讲的故事是从亚力史剑桥公司向复审委提出复审请求开始的,这个发明专利申请名为“人工程化抗B因子抗体”(申请号CN200880008123.2) ,其中,权利要求1请求保护的技术方案为:
1. 人工程化抗B因子抗体或其抗原结合片段,其在第三个短共有重复序列(“SCR”) 结构域内选择性结合B因子并防止C3bBb复合物的形成,其中所述抗体和其抗原结合片段的每一个包括选自下述氨基酸序列的Vκ和VH区:
a) 由SEQ ID NO:14的氨基酸序列组成的Vκ-区多肽和由SEQ ID NO:15的氨基酸序列组成的VH-区多肽;
b) 由SEQ ID NO:16的氨基酸序列组成的Vκ-区多肽和由SEQ ID NO:17的氨基酸序列组成的VH-区多肽;
c) 由SEQ ID NO:18的氨基酸序列组成的Vκ-区多肽和由SEQ ID NO:19的氨基酸序列组成的VH-区多肽;
d) 由SEQ ID NO:20的氨基酸序列组成的Vκ-区多肽和由SEQ ID NO:21的氨基酸序列组成的VH-区多肽;
e) 由SEQ ID NO:16的氨基酸序列组成的Vκ-区多肽和由SEQ ID NO:35的氨基酸序列组成的VH-区多肽;
f) 由SEQ ID NO:18的氨基酸序列组成的Vκ-区多肽和由SEQ ID NO:36的氨基酸序列组成的VH-区多肽;或
g) 由SEQ ID NO:20的氨基酸序列组成的Vκ-区多肽和由SEQ ID NO:37的氨基酸序列组成的VH-区多肽,并且其中所述其抗原结合片段选自Fab'、(Fab')2、Fv、scFv和双抗体,并且其中所述双抗体包括所述人工程化抗B因子抗体的VH和Vκ结构域——其由连接体连接,并且其中所述连接体非常短以至于不允许同一多肽的VH和Vκ结构域配对,而使所述VH和Vκ结构域与第二多肽的互补结构域配对以形成两个抗原结合位点。
本专利申请被驳回的理由是:权利要求1请求保护人工程化抗B因子抗体或其抗原结合片段,其中涉及a)-g)七个并列技术方案。但根据说明书的记载,构建获得的人工程化抗B因子抗体TA101-1、TA102-4和TA103-2的Vκ和VH区的序列的搭配是特定的,并且只有这几种抗体得到了实验验证的治疗效果,由于不同Vκ和VH区的搭配会影响抗体的特异性、亲和性等生理功能,也影响抗体的KD常数,因此本领域技术人员无法确定除了说明书中记载的几种特定的搭配组合外,其它的搭配组合是否能够达到本发明的目的,进而认为权利要求1没有以说明书为依据,得不到说明书的支持。
申请人提出复审请求并且没有修改权利要求,申请人认为,(a)-(d) 分别对应TA10、TA101-1、TA102-4和TA103-2的VK和VH区序列及其抗原结合片段,而(e) 、(f) 和(g) 是指在VH区的N-末端的第一位置处具有Q替换为E的TA101-1、TA102-4和TA103-2抗体的变体的VK和VH区及其抗原结合片段。由于mAb1379(即用于构建上述三种抗体的含有结合特异性决定簇的抗体,该抗体可以结合B因子) 的可变区与TA101-1、TA102-4和TA103-2的可变区之间的差异远大于由权利要求1的部分(e) 、(f) 和(g) 所陈述的抗体及其抗原-结合片段的Q替换为E的所产生的改变,同时说明书也教导Q替换为E促进产生更均匀的终产物(说明书第[0077]段) ,此外对人B因子具有高结合亲和力的TA10抗体的VH区中的N-端氨基酸残基就是E。因此,本领域技术人员将会预期,权利要求1中(e) 、(f) 和(g) 所请求保护的抗体及其抗原结合片段中Q替换为E的单个氨基酸残基的保守替换不会影响对B因子的结合亲和力,也不会显著改变免疫原性。因此,目前的权利要求1能够得到说明书的支持。
复审委受理此案后认为,本申请所要解决的技术问题是提供一种结合补体蛋白B因子并选择性抑制补体旁路(途径)的新型工程改造形式的单克隆抗体及其抗原结合片段。说明书中记载了权利要求1中a)-d) 技术方案所述抗体的亲和性实验及其结果,因此本案的焦点在于没有直接记载效果数据的(e) 、(f) 和(g) 所述的技术方案的技术效果是如何的,本领域技术人员是否依然能够认为其具有结合人B因子的功能。
复审委认为,本专利申请的说明书记载了足够证明(e)-(g) 技术方案所能达到的技术效果的内容。根据说明书附图图6(如下图所示) 的序列对比结果,N末端的残基Q既不位于CDR结构域内,也不位于典型地由抗体重链的CDR3内的序列和抗体轻链的CDR3内的序列代表的最小结合特异性决定簇(“BSD”) 中,而是位于FR1区。尽管抗体框架区的氨基酸可以通过影响抗体分子的正确折叠而影响抗体的亲和力,但由于谷氨酸和谷氨酰胺的分子结构较相似,并且都是亲水性残基,因此即使产生影响,影响的程度也十分微小。同时,TA10抗体的VH区的N末端氨基酸残基即为E,而TA10抗体对人B因子具有较好的结合亲和力,因此在没有相反证据的情况下,可以合理预期这种氨基酸残基的保守替换将不会导致抗体分子在三级结构上发生较大变化,氨基酸残基替换后的抗体也将具有与改造前的分子相似的结构和抗原结合活性。也就是说,可以预期权利要求1中e)-g) 技术方案所述抗体也将具有结合人B因子的功能。最终复审委做出了撤销驳回的决定。
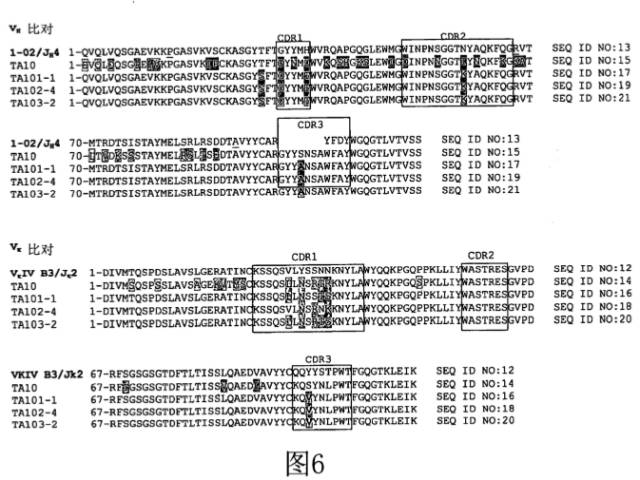
TiPLab磨杵君觉得,上面的故事直接说明了说明书(包括说明书附图) 所记载的内容对克服支持问题的重要性。若不是说明书附图确切地记载了替换氨基酸在整个抗体结构中的位置,就无法从本领域技术人员知悉的公知常识的角度说明这种替换对结合抗原的亲和力的影响程度是极为有限的;同样地,若不是说明书中确切地记载了Q替换为E是为了使抗体更稳定可靠,结合亲和力提高,同时记载了该氨基酸位点上为E的效果优于Q的效果的实验结果,就无法确切地证明替换为E还能够达到结合人B因子的技术效果。
在说明书恰到好处的情况下(这里的恰到好处是指没有机械地把所有的技术方案全部都一一对应地做一遍实验,但是把今后可能会涉及支持问题时能够用于争辩的道理和实验数据都完完整整地记载清楚了) ,可以通过说明书本身记载的内容(这种内容有个高大上的名称叫“内部证据”,它的效力还高于搜集的用于证明自己观点的文献、教科书等“外部证据”) 完整地形成一个争辩得到说明书支持的观点和相应的逻辑和证据,这样,就可以在所谓的少补实施例和较大的保护范围之间寻找一个可能的平衡。
当然,TiPLab磨杵君还需要指出的是,为了克服潜在的支持问题,在说明书中啰啰嗦嗦地说了一大堆机制机理也是存在风险的,这是应为过于“直接”过于事无巨细地叙述技术方案会导致审查员认为该技术方案没有创造性,因此很多时候支持问题本身还与创造性之间存在着平衡关系。

可见在专利申请实务中以上的两种平衡也都需要在专利申请文件撰写时提前做好谋篇布局,这对发明人准确地阐述自己的技术方案和代理人准确地领会并反映在合适的保护范围和合适的说明书记载内容上的要求确实还是比较高的。