
首个PD-L1纳米抗体
本文介绍康宁杰瑞开发的PD-L1抗体KN035-Fc,该药物已经在前不久相继在中美获批临床。国际上,罗氏的PD-L1抗体AtezolizumabPD-L1已经在2016年获得FDA批准上市,用于治疗膀胱癌。默克/辉瑞的PD-L1抗体Avelumab已于2017年3月获得FDA批准上市,用于治疗皮肤癌。阿斯利康的PD-L1抗体Duvarlumab则处于临床后期阶段。
小编专文介绍KN035-Fc有两个原因,第一,该药物与前几个PD-L1抗体均有所不同,是一种纳米抗体-Fc融合蛋白,结构上具有明显的差异;第二,康宁杰瑞在专利与文献中均披露了较为详细的药学信息和临床前研究数据,这对于习惯炒作概念、谈数据则语焉不详的国内新药研发环境来说,实在是一股清流。说到底,新药的好坏、有无差异化特色,还是要看数据来说话。国内的新药研发,需要更多康宁杰瑞这样的实干派。
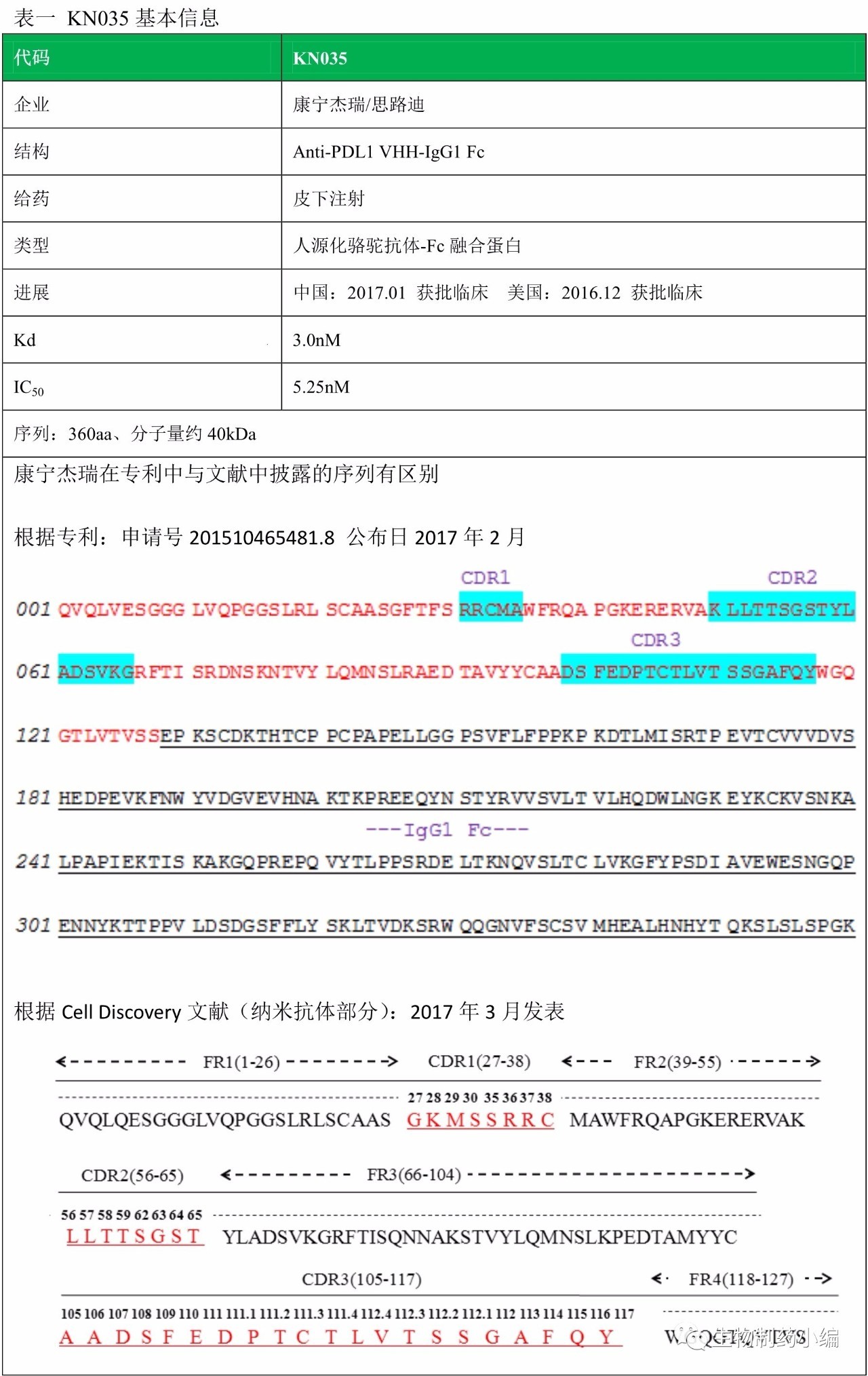
关于序列,康宁杰瑞在专利201510465481.8中的介绍,噬菌体库筛选后确认了56号纳米抗体,该序列与Cell Discovery的序列仅差一个氨基酸:123位。但康宁杰瑞在专利中对56号纳米抗体进行了人源化改造,并明确提到其中一个人源化Hu56V2-Fc即为KN035,而Hu56V2-Fc改变了十余个氨基酸,与Cell Discovery序列差别较大。小编分析可能康宁杰瑞在序列优化的时间和流程较长,在序列等方面出现了一些变化,因此出现一些矛盾。从时间来看,文献发表时间更晚近一点(专利申请时间为2015年11月,文献投稿时间为2016年11月),KN035的序列似乎更可能为Cell Discovery中披露的序列。但为什么不需要进行人源化,还不清楚。考虑到序列的矛盾,其IgG1 Fc也可能有序列突变的可能(采用强ADCC或弱ADCC,是两种不同的粗略),因此KN035-Fc的序列仍需期待进一步的公开信息以确认。
专利中披露的研发过程
在2017年2月15日公开的专利201510465481.8中,康宁杰瑞描述了PD-L1抗体KN035-Fc的详尽筛选流程。CHO表达重组PD-L-Fc,用PD-L1-Fc四次免疫新疆双峰驼,分离100ml外周血提取总RNA,反转录得到cDNA文库,然后克隆建立噬菌体展示文库,库容达1.33*108。
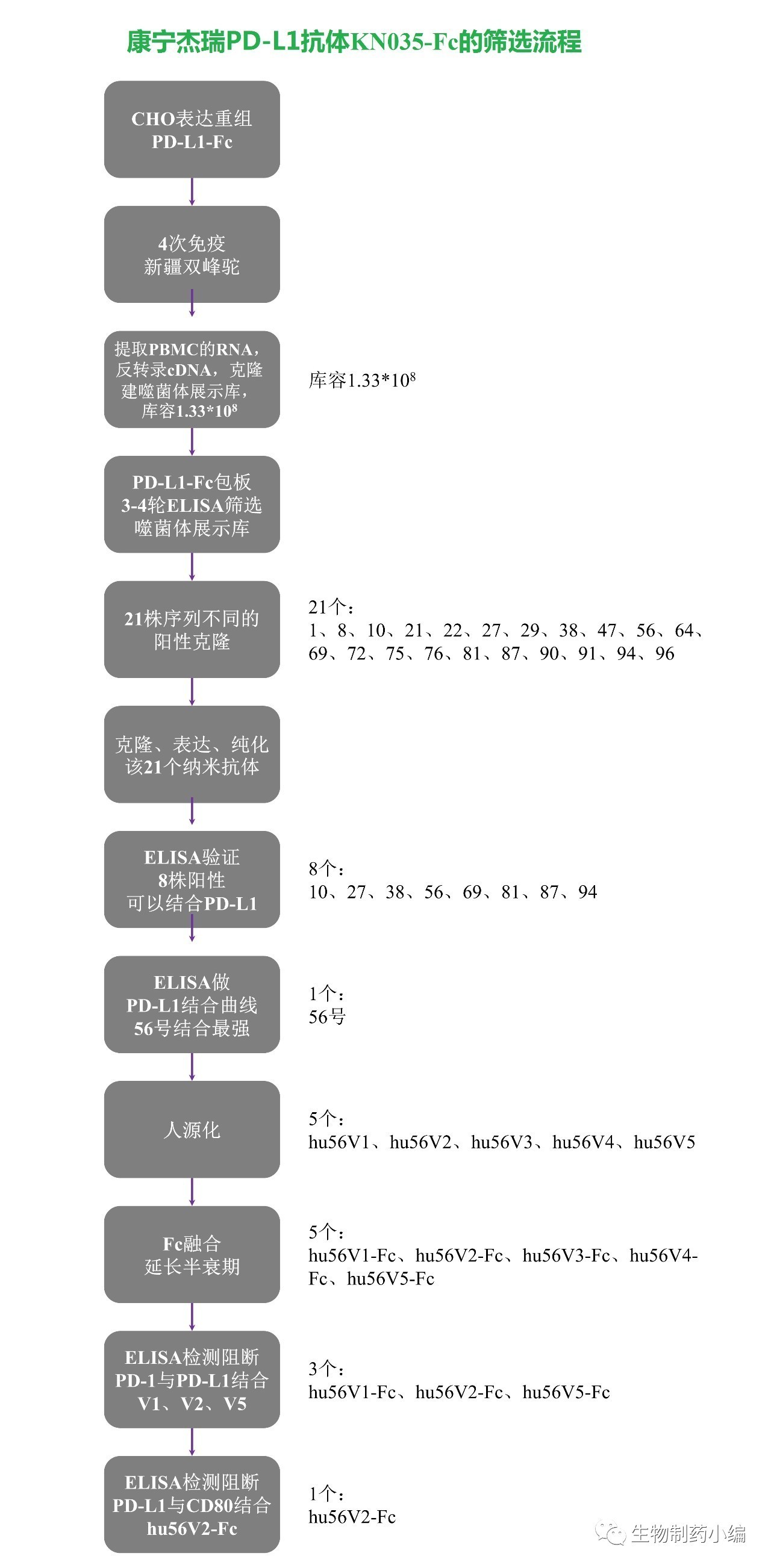
整个筛选过程基于ELISA,3-4轮PD-L1包被的ELISA筛选,共得到21株序列不同、可结合PD-L1的阳性克隆。将这21株克隆的基因进行重组表达,纯化得到21个纳米抗体。ELISA结合验证,得到8株阳性克隆。这8个纳米抗体,通过ELISA分析与PD-L1结合曲线,发现56号亲和力最强,IC50为143ng/ml。

注:灰色底纹为人源化改造的位点,黑色底纹为与cell research披露序列不同的位点。
随后进行人源化改造,得到5株变体并进行Fc融合以延长半衰期。通过ELISA分析阻断PD-1与PD-L1、PD-L1与CD80的结合能力,确认Hu56V2-Fc为候选药物,也即KN035。(专利原文提到,但序列与Cell Discovery披露序列有差异)
文献中披露的药学数据和表位研究信息
2017年3月Cell Discovery发表了康宁杰瑞与上海交通大学周爱武教授等人合作的、关于KN035与PD-L1的结构解析的文章,披露了一些重要的药学信息。
稳定性好
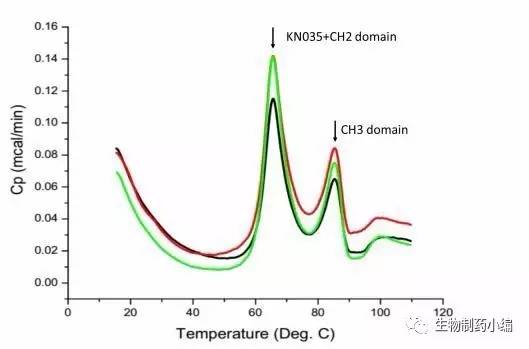
微量热DSC检测,KN035-Fc的热变性温度为66℃左右,决定了KN035-Fc可以常温保存,结合皮下注射的便利,很大程度上将提高患者的依从性。
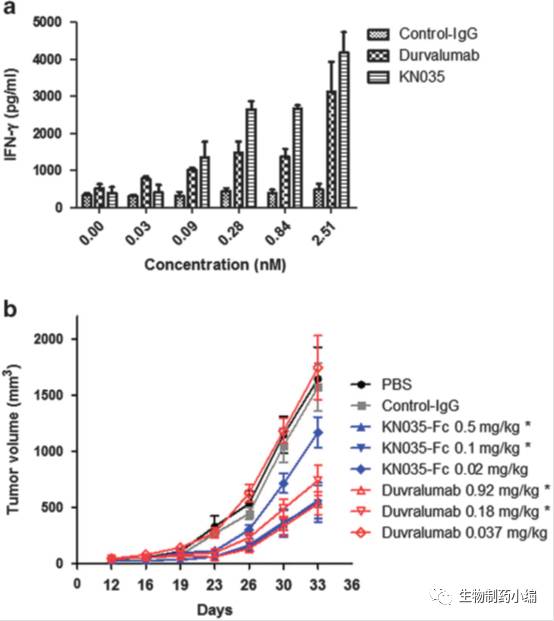
ELISA检测阻断PD-1与PD-L1相互结合的能力,发现KN035-Fc的竞争活性(EC50=2.5nM)略高于阿斯利康的PD-L1抗体Durvalumab(EC50=3.1nM)。

KN035-Fc刺激T细胞分泌IFN-γ的能力略高于Durvalumab,体内抗肿瘤活性则与同等摩尔浓度的Durvalumab相当(注意,由于KN035-Fc不结合鼠源PD-L1,所以体内抗肿瘤活性的检测使用人PBMC与KN035-Fc同时注射的方法,通过激活人PBMC中的T细胞,来杀伤鼠的移植肿瘤细胞)。
结构生物学研究揭示抗原结合表位
康宁杰瑞与上海交通大学医学院的周爱武教授等人合作,解析了KN035-Fc与PD-L1的结合位点,该研究结果发表在2017年3月的Cell Discovery上。
KN035与PD-L1的结构如下:
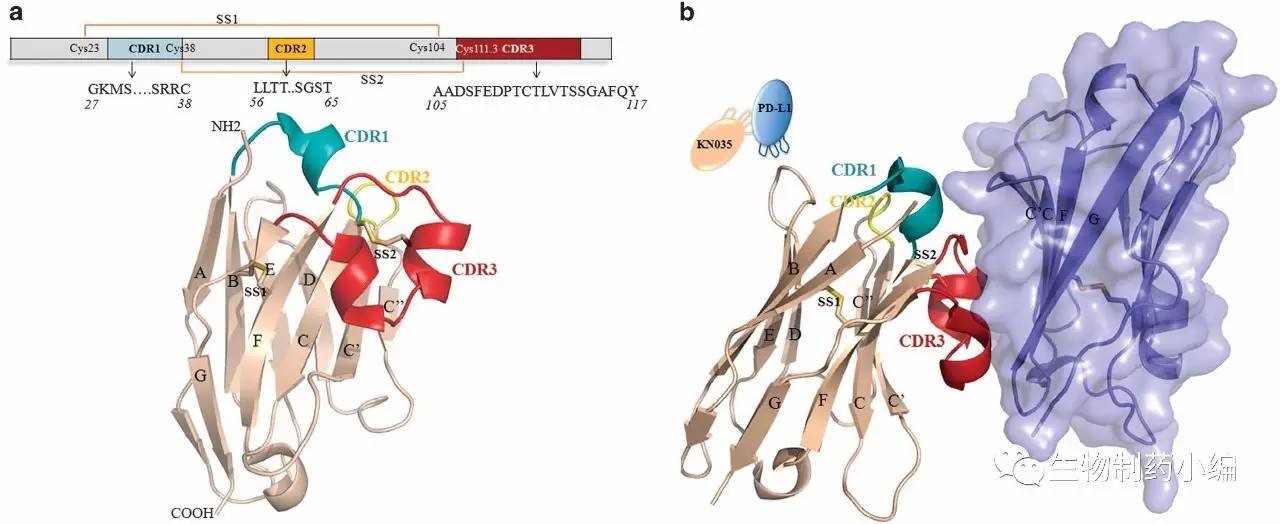
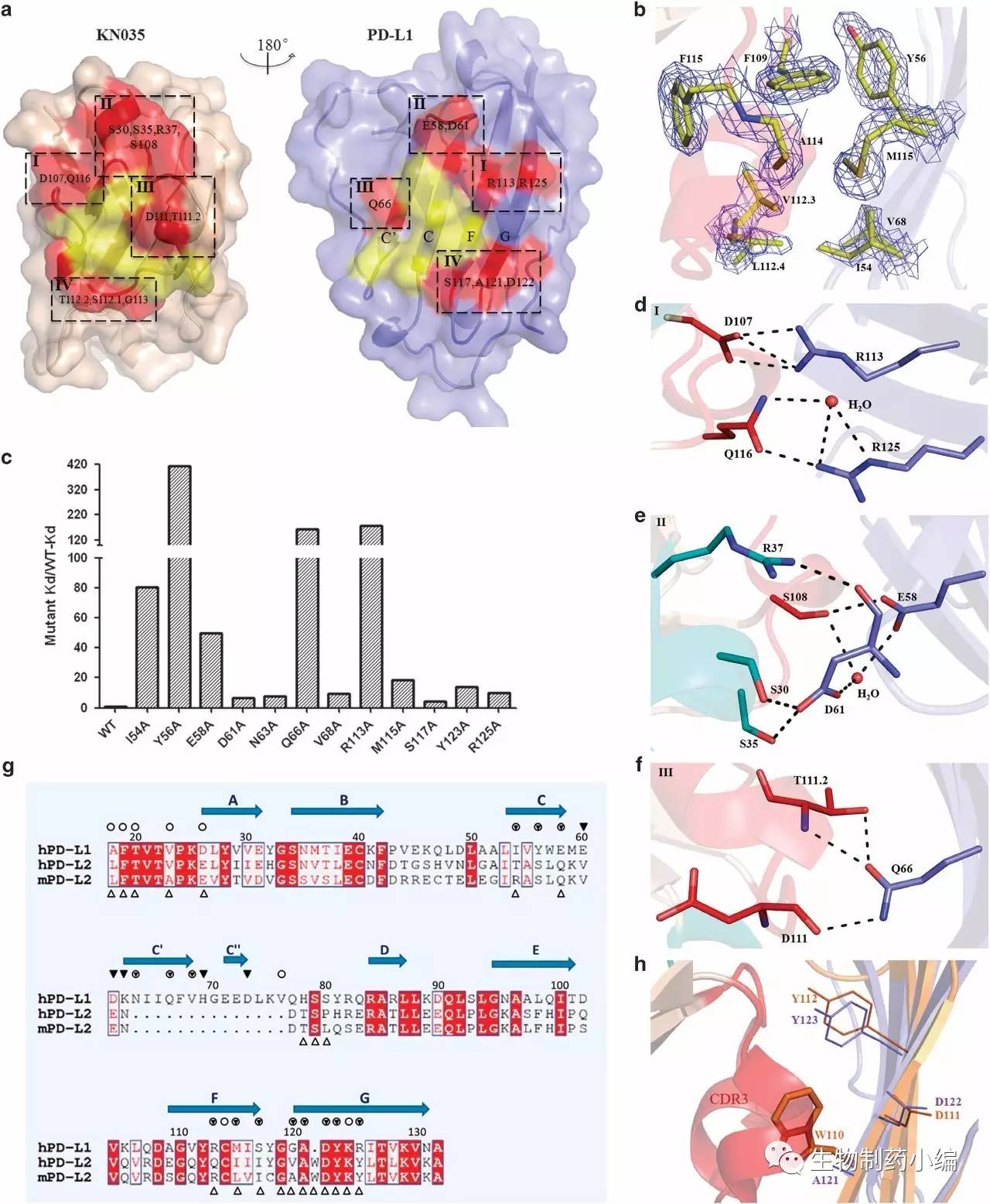
如下图a,KN035和PD-L1表面存在互补的疏水域(黄色)和亲水域(红色)。下图b的电荷密度图则标出了左侧KN035的F109苯酚环与F115芳香烃环及右侧PD-L1的Y56芳香烃环堆积在一起。
如下图,PD-1通过C、C’、G、F Strand与PD-L1结合,而KN035则通过CDR1、CDR3与PD-L1结合。
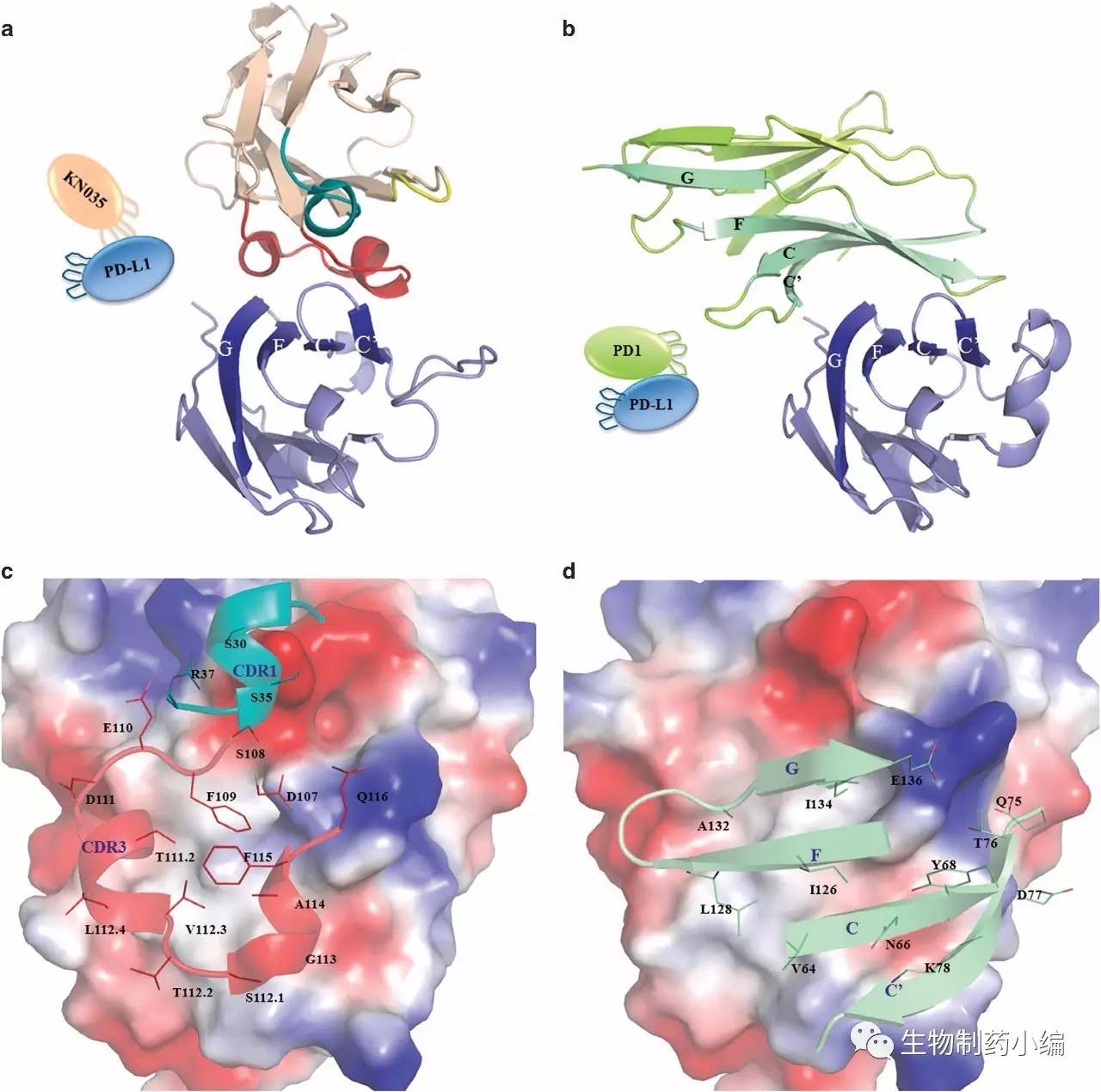
PD-L1的表面比较平,KN035与PD-L1的结合主要通过CDR3实现,这种作用同时来自于疏水相互作用和电荷相互作用力。KN035的nM级亲和力源于每个氨基酸都参与了相互作用,贡献了部分亲和力。噬菌体展示库提供了筛选的基数、ELISA等亲和力筛选方法提供了筛选的手段、结构生物学研究则揭示了这种亲和力的结构基础。PCSK9表位专利大战表明表位专利日益重要,对于越来越多加入国际竞争的国产新药来说,也要适应这种趋势。药学研究需要更加透彻,知识产权布局也须更加谨慎。
小编总结
尽管在抗体筛选方面,KN035的开发可能尚不如剑桥抗体技术中心(CAT)在世纪初开发阿达木单抗、贝利木单抗时候动辄筛选上千个抗体那么复杂、系统,但相对于国内药企来说,已经是难能可贵。此外在纳米抗体定位、靶点选择、药学研究、临床前评估方面都做了踏实的工作且不乏创新。
总的来说,康宁杰瑞KN035的开发具有一定的开创意义,差异化特色与创新都将成为一个标杆,但更可贵的是其务实的创业精神与开放的态度。近年来国内生物医药投资火热,药企新概念炒作不断,谈数据则往往语焉不详,很多连药物大概结构都不清楚。中国生物医药若要取得长足进步,不仅要紧跟前沿,也要摒弃伪创新,摒弃概念炒作,踏踏实实做好眼下的工作。
参考资料
中国专利 201510465481.8
Structural basis of a novel PD-L1 nanobody for immune checkpoint blockade(2017)