
由苏州康宁杰瑞生物科技有限公司(康宁杰瑞)开发的重组CTLA-4变体Fc融合蛋白注射液(KN019)于日前获得中国国家食品药品监督管理总局颁发的临床批件。
KN019项目是美国施贵宝公司Nulojix(INN通用名:belatacept)的生物类似物,是人细胞毒性T淋巴细胞相关性抗原CTLA-4胞外区变体(A29Y和L104E)与Fc片段的融合蛋白,分子结构复杂,很难仿制。Nulojix能够与抗原递呈细胞表面的CD80/CD86结合,抑制T细胞的活化和增殖,具有免疫抑制作用。其适应症为:经巴利昔单抗诱导,与麦考酚酸酯和皮质激素联用,用于在接受肾移植的成年患者中预防器官排斥。Belatacept有多个N和O糖糖基化修饰,且翻译后修饰与其功能密切相关,其复杂的生产工艺和质控极具挑战性。康宁杰瑞研制的KN019项目中试生产得率高,蛋白的一级结构、高级结构和翻译后修饰与原研药Nulojix高度相似,药理毒理研究结果也与Nulojix的结果高度一致,有望成为Nulojix的国内首仿及独家药品。
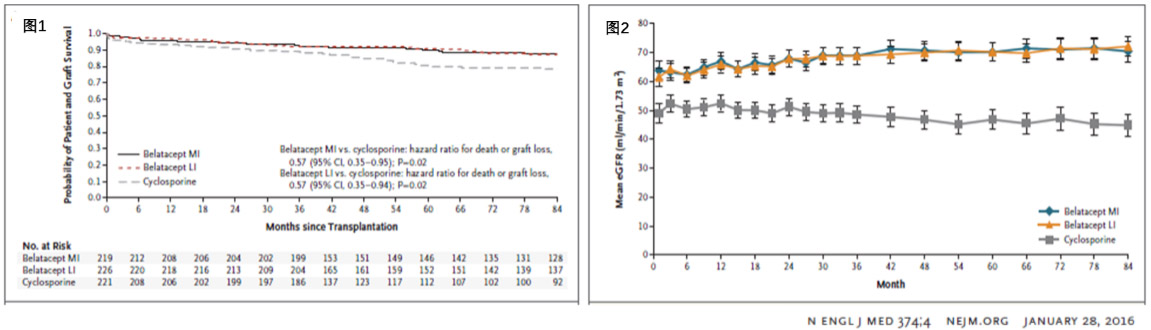
接受肾移植的患者需要终身用药来预防自身免疫系统排斥移植器官,目前主要是以钙(调)磷酸酶抑制剂(CNI)为基础的免疫抑制疗法,虽然能够降低急性排斥率和提高患者早期生存率,但是其对肾脏、心血管系统的毒副作用造成患者的长期生存率并不高。相比较,belatacept的作用靶点清晰,毒副作用较低,不但保持了较低的急性排斥率,而且在长期用药方面具有显著的优势,患者和移植器官的长期生存率显著高于以CNI(CsA)为基础的免疫抑制治疗(如图1),所移植肾脏的功能也长期保持良好并显著高于对照组(如图2)。
关于康宁杰瑞
苏州康宁杰瑞生物科技有限公司由徐霆博士2008年归国创建,在苏州设立研发中心6000余平方米,并成立博士后工作站。8年多来,建立了多个具有自主知识产权的生物大分子药物研发平台,包括生物大分子高效表达平台,抗体筛选平台、双特异抗体平台和混合抗体生产平台。能够完成从抗体/蛋白药物早期筛选和工程化、成药性评价、细胞株构建和小试工艺、到中试放大及临床试验用药的生产及分析质控等全部流程。公司目前拥有多条cGMP生物大分子药物中试生产线和无菌制剂灌装车间。康宁杰瑞在研的生物大分子新药有十多个,已经申报临床批件8项,其中2项正在临床研究阶段(1项正在进行国际多中心开发)。康宁杰瑞位于江苏苏州的生产基地已启动建设,计划2019年投入使用,力争在不久的将来为患者提供更多高效、优质、价格合理的治疗药物,解决国内药物可及性的同时积极参与国际竞争。
欲了解更多信息,请登录网站:www.alphamab.com