抗体药物目前是生物医药行业中最具前景的领域之一,TiPLab磨杵小分队研究了专利复审委员会于2015年及2016年作出的100件相关复审和无效审查决定,并对它们逐一进行了分析和统计。
洞见
专利保护抗体发明的挑战和策略(一)

by
TiPLab磨杵小分队
抗体药物大部分是针对特定靶点的生物药,其具有较高的特异性、有效性和良好的安全性。抗体药物目前是生物医药行业中最具前景的领域之一,截止2016年,中国的单克隆抗体药物市场容量就已达80多亿元。而在单克隆抗体基础上进一步改进的融合蛋白(如双特异性抗体)和与治疗剂(如细胞毒素)偶联的抗体-化学药偶联物(ADC),也具有十分广阔的发展空间。
面对如此可观的市场,对生物医药企业尤其是原研药开发企业而言,采用申请专利的手段保护抗体药物是未来获取丰厚的财富回报的最可靠的保障之一。而对仿制药开发企业而言,合适的专利布局仍能为其在激烈的市场竞争中获得权益。可见获得状态稳定、保护范围合理的专利权对医药企业具有至关重要的意义。那么,根据中国的专利审查和司法实践,生物医药企业在为抗体药物相关发明寻求专利保护的过程中最常遇到的挑战有哪些呢?在专利申请文件的准备过程中又该注意哪些问题呢?TiPLab磨杵君将尝试通过一系列短文中的几个小故事来与大家共同探讨以上的问题。
为了利于对全局进行把握,刀客特张建议TiPLab磨杵君先对目前抗体相关发明在中国进行专利申请的情况进行全面调查。
TiPLab磨杵君的调查结果显示,截止2016年,约有41500件抗体相关发明已经向国家知识产权局提出了发明专利申请,其中约有14000件已经被授予了专利权。在这广袤的专利申请的海洋中,有近300件还进入了复审或无效的阶段,这些专利申请至少经过了审查员和复审委这样两批专业人士的审查,无效案件更是还获得了竞争对手的特别关照,因此具有更大的参考价值。TiPLab磨杵君精心挑选了专利复审委员会于2015年及2016年作出的100件相关复审和无效审查决定,并对它们逐一进行了分析和统计。结果显示,在2015~2016年位列前三的法律问题依次为:《专利法》第二十二条第三款、第二十六条第四款和第三十三条。此外,《专利法》第二十二条第二款、第二十六条第三款和第三十一条第一款也是较为常见的法律问题。
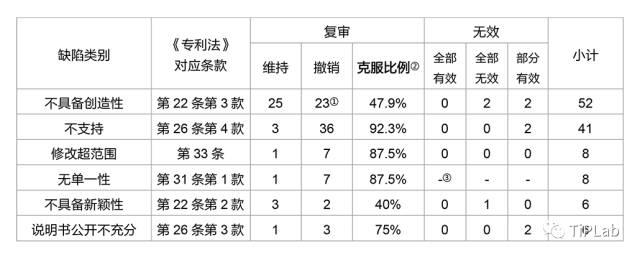
▲ 调查结果
①部分复审案件和无效案件存在涉及两条或以上法律条款的情况,表1按照法律条款进行统计,产生了总数大于100的结果。
②克服比例的含义为涉及某一法律条款的所有复审案件中,最终复审决定为撤销驳回决定的案件占这些复审案件的百分比。
③无单一性的缺陷不属于无效请求和宣告无效的理由。
TiPLab磨杵君认为,在抗体相关发明的专利申请过程中频繁遇到上述的“高危”法律问题与抗体本身的结构性质存在着一定的关系。众所周知,抗体的特异性是通过重链可变区和轻链可变区中的互补决定区(CDR)与抗原的特异性结合而实现的,因此一般以结构特征(这也是最为可靠的限定方法之一)来限定抗体,即通过6个CDR区域或者轻链和重链的氨基酸序列来限定所保护的抗体。同时为了尽可能地扩大保护范围,在用氨基酸序列进行限定时通常还会采用“同源性达到百分之若干”的语言进行描述。此外,很多抗体的可变区甚至恒定区的一些位点的氨基酸发生了突变,因此还会使用“X区域的X位的X氨酸突变为X氨酸”的语言进行限定。在如此“云里雾里”的结构特征的限定下,还会出现各种限定的技术特征的排列组合。这样看来,抗体的结构特征确实好复杂,很容易产生不匹配的情况,即权利要求保护一个很大的、含有很多种排列组合的范围,而说明书中记载的有靠谱数据的实施例仅能体现很少数的、具有特定氨基酸序列的抗体所产生的效果。这时,就可能会被审查员认为含有了大量“推测”的内容,产生所谓“权利要求书得不到说明书支持”的问题,即被认为违反了专利法第二十六条第四款的规定。但是,广大的生物医药企业的成本是宝贵的,广大的科研人员的时间精力是有限的,不太可能为了补充足够数量的实施例而面面俱到、夜以继日地疯狂做实验,在这种情况下,选择合适且有价值的保护范围和撰写具体且有层次的说明书就是尽量避免这一问题的有利武器。
另一个不太可能回避的问题是,目前获得一个全新的抗体的靶点是一件比较困难的事情。如果保护一个完全全新的靶点,只要能证明该靶点的抗体能产生一定的技术效果,那么基本上不用太担心这类发明的创造性问题。可是这样的抗体毕竟不是太多(一般称之为原创型发明),更多的抗体相关专利申请本质上是对前人工作成果的进一步改进(一般称之为改进型发明),有进行序列变化的,有进行修饰等结构改造的,有和化疗药物联合用药的,有制备不同剂型的。在这种情况下,当审查员检索到了所谓的“最接近的现有技术”后,能不能说服审查员不要把大家辛辛苦苦得到各种改进的特征统统认为是“本领域常规技术手段”,从而使改进的效果逃离惨遭无视的悲惨命运呢?对此,《审查指南2010版》曾教导通过使“发明进一步由其他特征等限定,并因此使其产生预料不到的效果”来说明抗体尤其是已知抗原的单克隆抗体的创造性。但是大家所认为的抗体药物取得的好效果是否是所限定的特征带来的呢?是否又达到了《审查指南》中所谓“预料不到”这样层次的好效果呢?诚然,这种评判中存在着一定的主观因素,但通过对典型案例的分析,可以获悉一些原则和思路,从而尽量通过讲机理、找证据、改权利要求等诸多手段来针对创造性问题进行争辩。
同时,在进行实质审查答复OA、提复审、答复复审通知书甚至在无效阶段时,往往还会发生以下的悔悟:要是说明书还写着XX就好了,早知道XX就根本不要提了。有时候修改时需要限定内容,却发现无论是原始的权利要求书还是说明书都没有什么确切相关的记载,稍微一改动就违反了专利法第三十三条的规定。有时候,争辩创造性却发现有些记载的内容让人很难自圆其说,甚至在对比文件的技术方案的逼迫下出现了可怕的矛盾。对此,TiPLab磨杵君认为申请文件撰写的水平高低固然是重要的因素,但是总的谋篇布局还得建立在熟悉整个技术领域,深入掌握本发明技术方案的基础上。可见专利申请的“事前”准备,对整个领域现有技术的正确划界,对发明点的着重阐述和层次保护都十分重要,并且这对后续顺利获得授权以及在授权后保持权利的稳定性也十分重要。
由上所述,是否觉得抗体相关发明的专利保护真是比较复杂呢。好了,话休烦絮,TiPLab磨杵君将在本系列接下来的几篇文章中尝试总结应对这些挑战的策略。

© 本文版权由TiPLab & Biotitude所有,欢迎个人转发,其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:生物制药小编”。