
近年来,肿瘤免疫疗法取得长足进展,Opdivo、Keytruda为代表的免疫检验点抑制剂在肺癌、黑色素瘤等多瘤种取得突破性进展。从而开启了整个肿瘤免疫的大门,继PD-1/PD-L1,更多的抑制或共刺激信号通路的相关靶点成为研发热点。
PD-1/PD-L1引发肿瘤免疫研发热潮
免疫细胞的功能受到紧密调控,在遇到外源抗原的时候,会通过一系列共刺激信号被激活;同时也会通过一系列共抑制信号被抑制功能,以免发生自身免疫及组织损伤。这些共刺激信号或者共抑制信号,共同组成免疫检验点,调控免疫细胞的功能。许多癌细胞会通过免疫检验点信号通路来逃避免疫细胞的杀伤,PD-1/PD-L1就是已经大获成功的免疫检验点抑制剂抗体,通过解除癌细胞的免疫逃逸,重建了免疫细胞对癌细胞的杀伤作用。
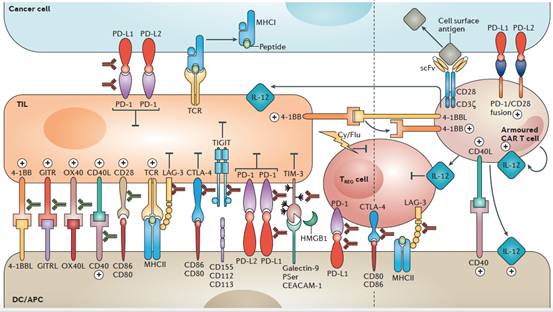
▲ 免疫检验点调控
免疫检验点抑制剂中,PD-1/PD-L1已经获批5个抗体药物,其中PD-1抗体Opdivo、Keytruda最为成功。2017年,5个PD-1/PD-L1抗体合计销售额100亿美元,2018年上半年合计销售额达到71.68亿美元,一举超越HER2、VEGF/VEGFR靶点成为仅次于TNFα的第二大抗体药物靶点。
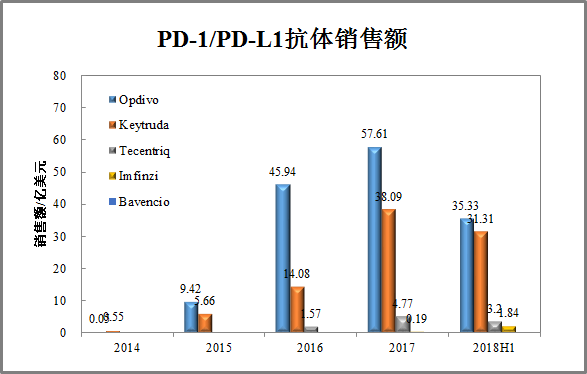
▲ PD-1/PD-L1抗体销售额(注:Opdivo含小野制药在日本市场销售额3.95亿美元)
PD-1/PD-L1的成功,引发了肿瘤免疫的研发热潮。免疫检验点抑制剂抗体药物靶点,除了CTLA-4、PD-1/PD-L1 ,TIM-3、TIGIT、VISTA等也在积极开发。与此同时,免疫检验点的激动剂抗体的研发竞争,也愈来愈激烈。
免疫检验点激动剂
CTLA-4、PD-1是B7-CD28家族的共抑制性受体,而CD28(CD28家族的名称来源)则是B7的共刺激性受体,ICOS则是被ICOSL激活的另外一个共刺激性受体。CD28和ICOS下游信号通路的激活,会驱动T细胞的激活。近年来该领域取得了突破性进展,CD28、ICOS的激动剂抗体也成为癌症治疗的研发靶点。另一个大家族是TNFR家族,该家族29个受体中有6个被证实是作为共刺激性信号存在:TNFRSF5(CD40)、TNFRSF4(OX40)、TNFRSF9(4-1BB)、TNFRSF7(CD27)、TNFRSF18(GITR)、TNFRSF8(CD30)。
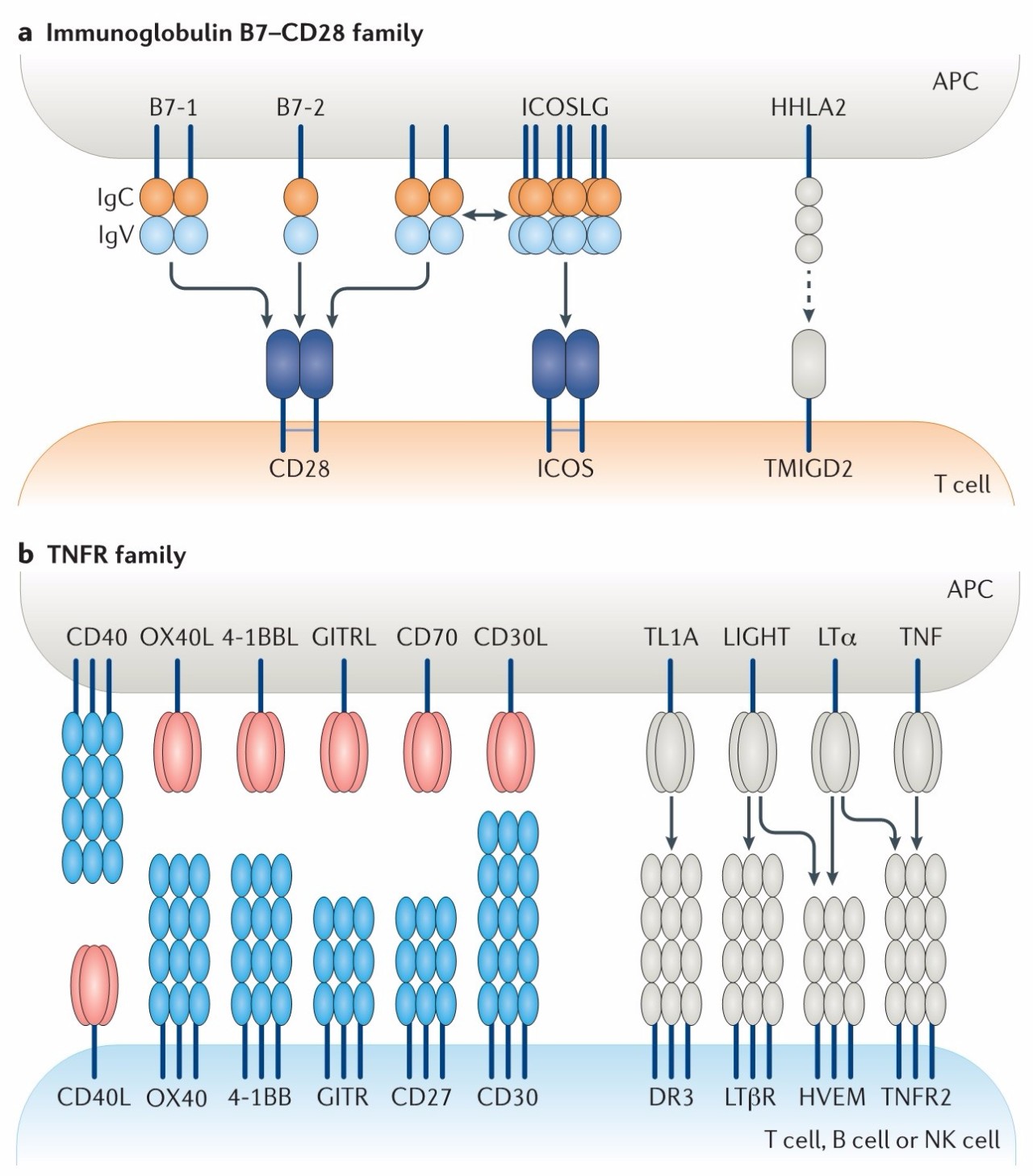
▲ B7-CD28家族和TNFR家族共刺激受体
激动剂抗体的研发
抑制剂抗体一般只需筛选亲和力最高的、与配体竞争性结合的抗体即可。而激动剂抗体的筛选通常没有通用的规则,因为激动剂抗体与受体的相互作用受多种因素影响:结合表位、亲和力、valency(价)、degree of receptor occupency(受体占有度)、Fc与FcγR的相互作用、化学计量学等。因此,激动剂抗体的筛选多通过细胞或体内的功能性实验来筛选。尽管如此,对于天然配体-受体复合物的结构信息和结合信息的了解,一定有助于针对特定受体设计激动剂抗体。
以valency(价)为例,研究发现一些配体与受体的相互作用是基于三聚体形式发挥作用的,有一种颇受认可的假说即很多配体与受体的相互作用都是基于这种形式。如TNFR与配体的作用,有几种理论均基于TNFR的三聚化和TNF配体的三聚化,还有一种假说认为在此基础上,TNF三聚体桥联多个TNFR三聚体,进而形成超大复合物,以激活下游信号通路。如一些研究发现CD28、CD40、OX40、4-1BB的激活都需要FcRIIB,而FcRIIB明显不会传导到胞内信号,合理的解释即为其介导受体形成超聚物。值得一提的是,成都三叶草生物一举核心技术蛋白三聚化技术Trimer-tag®,研发了靶向4-1BB的SCB-333(4-1BBL-Trimer)和靶向OX40的SCB-340(OX40L-Trimer)。尽管不是抗体类药物,但其配体设计技术值得研发激动剂抗体的药企借鉴。
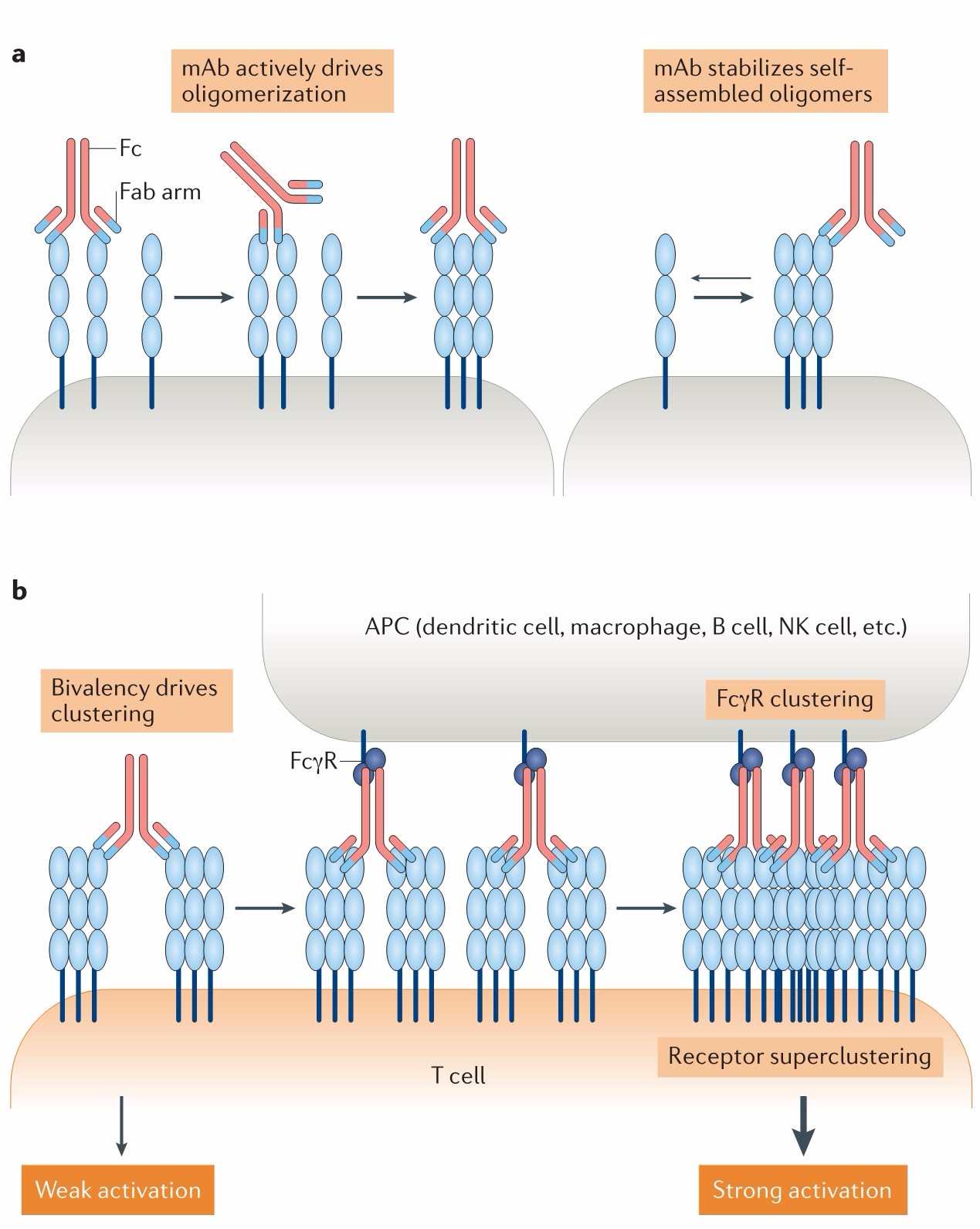
▲ 激动剂抗体介导TNFR受体超聚物的形成
再以化学计量学为例,理想的情况是受体与激动剂抗体的摩尔比接近1:1,介导超聚物的形成。如果受体远多于激动剂抗体,将缺乏足够的抗体桥联受体;如果激动剂抗体远多于受体,则同样无法桥联足够的受体。
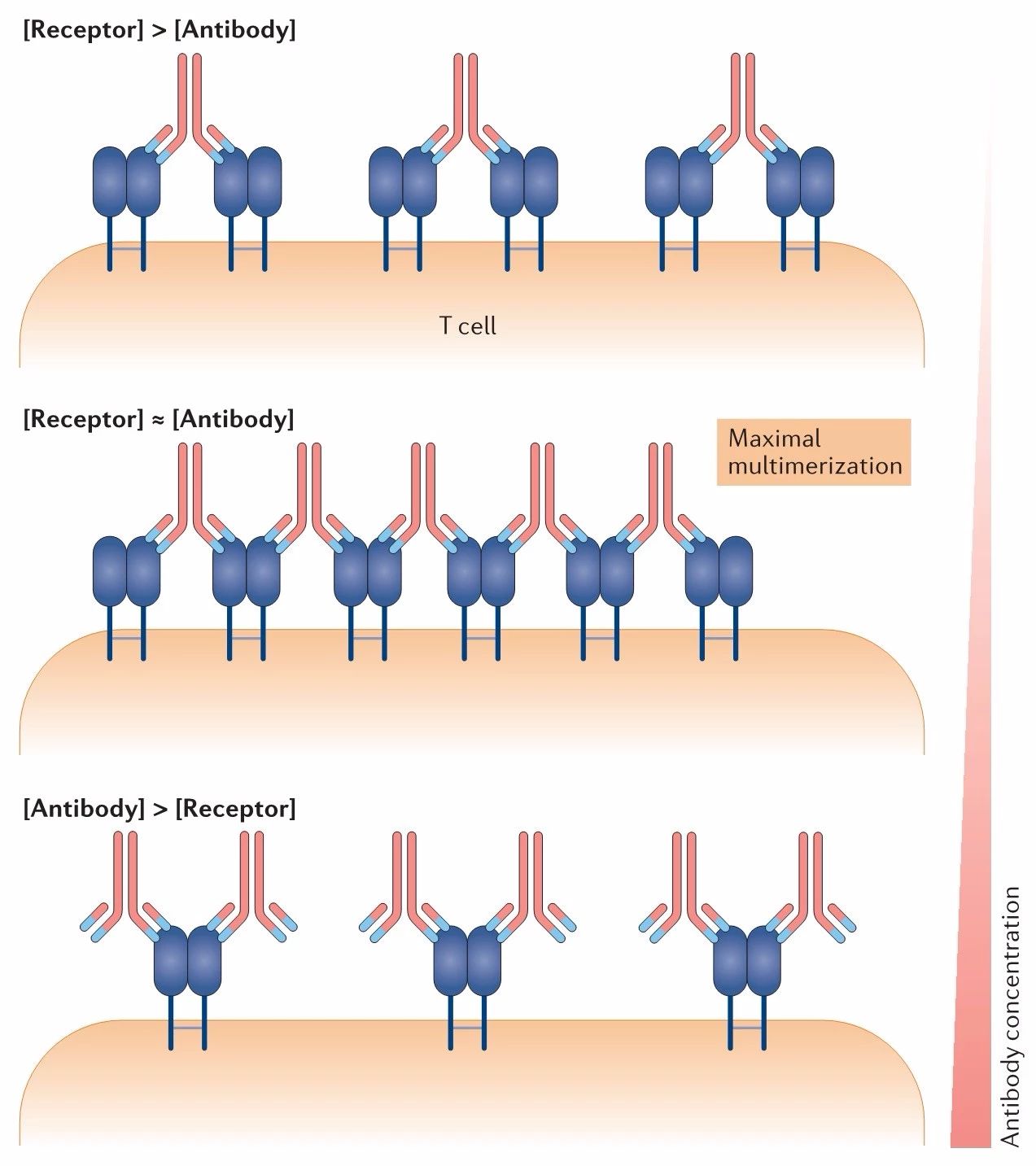
▲ 激动剂抗体的作用受化学计量学影响
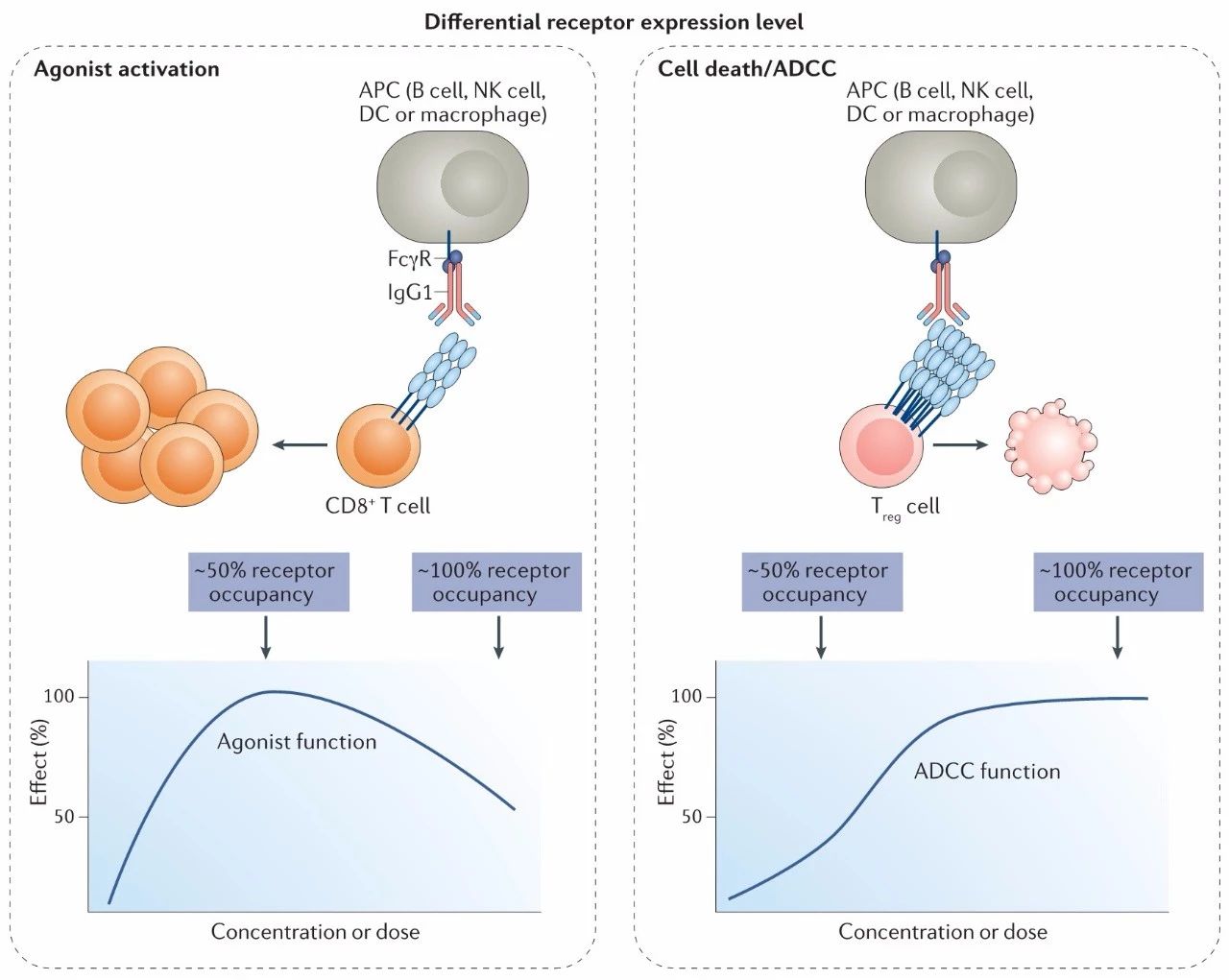
此外,Fc效应子功能与激动剂功能的平衡,也是激动剂抗体开发的重要考量因素之一。因为FcγR介导了受体超聚物的形成,对于抗体激动剂是必须的,但FcγR亲和力最高的IgG1,同时也意味着最强的ADCC作用。激动剂效应与给药剂量的关系呈钟型曲线;ADCC效应与给药剂量的关系则呈S型曲线。对于CD8+ T细胞,需要其激动剂效应,激活该细胞,杀伤肿瘤细胞。对于Treg细胞,需要其ADCC效应,杀死Treg细胞,解除对杀伤性T细胞的负调控。重要的是,关于不同T细胞种类的受体表达水平数据还不够,因而对激动剂效应的ADCC效应的调控也就更加复杂。
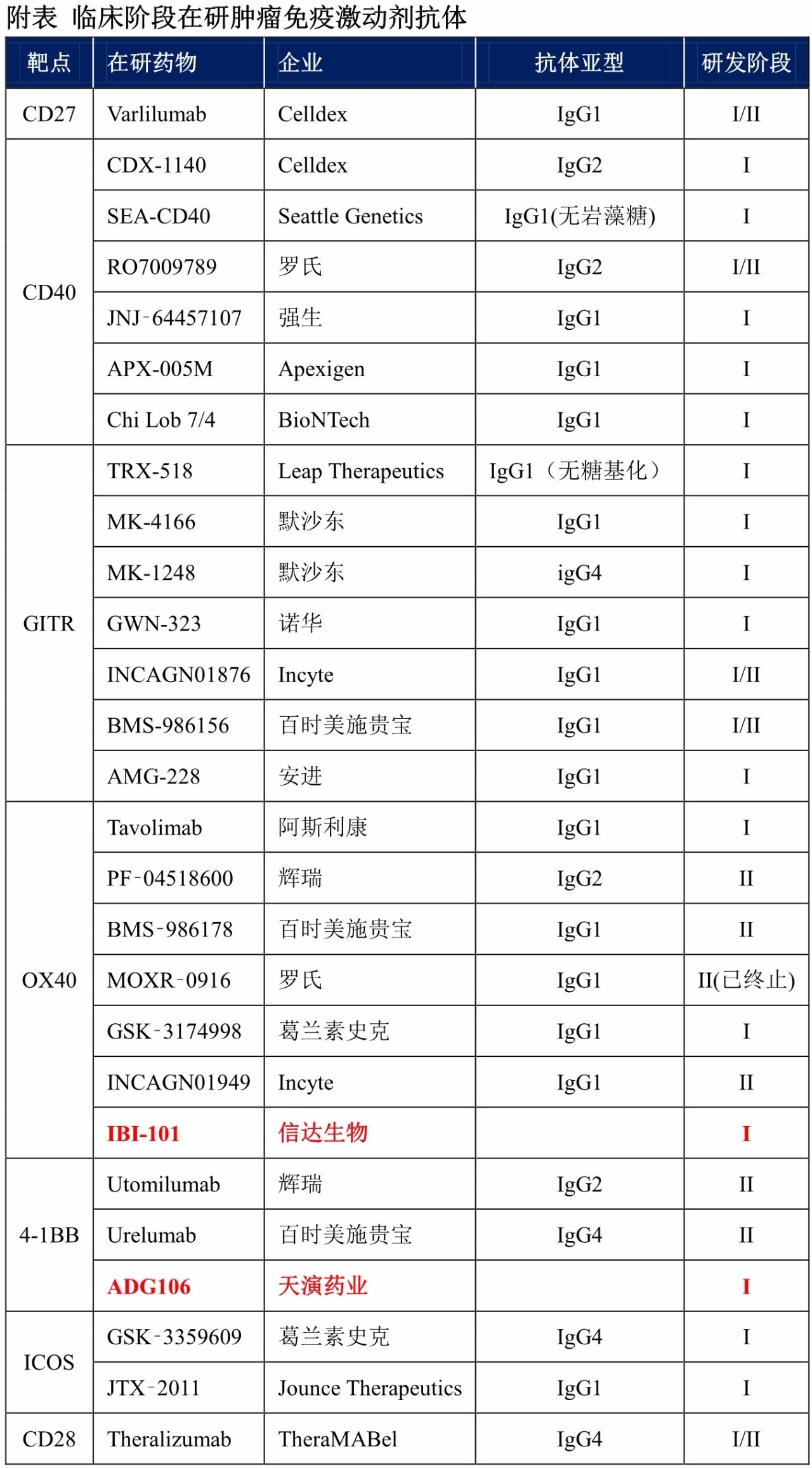
处于临床阶段的免疫检验点激动剂抗体药物
CD40、OX40、GITR、4-1BB等是目前研发竞争最为激烈的免疫检验点激动剂抗体靶点,罗氏、默沙东、辉瑞、百时美施贵宝、Incyte、Celldex等药大小药企均积极进入该领域。多数免疫检验点抑制剂抗体均采用强ADCC作用的IgG1亚型,少数采用了IgG2或IgG4亚型。
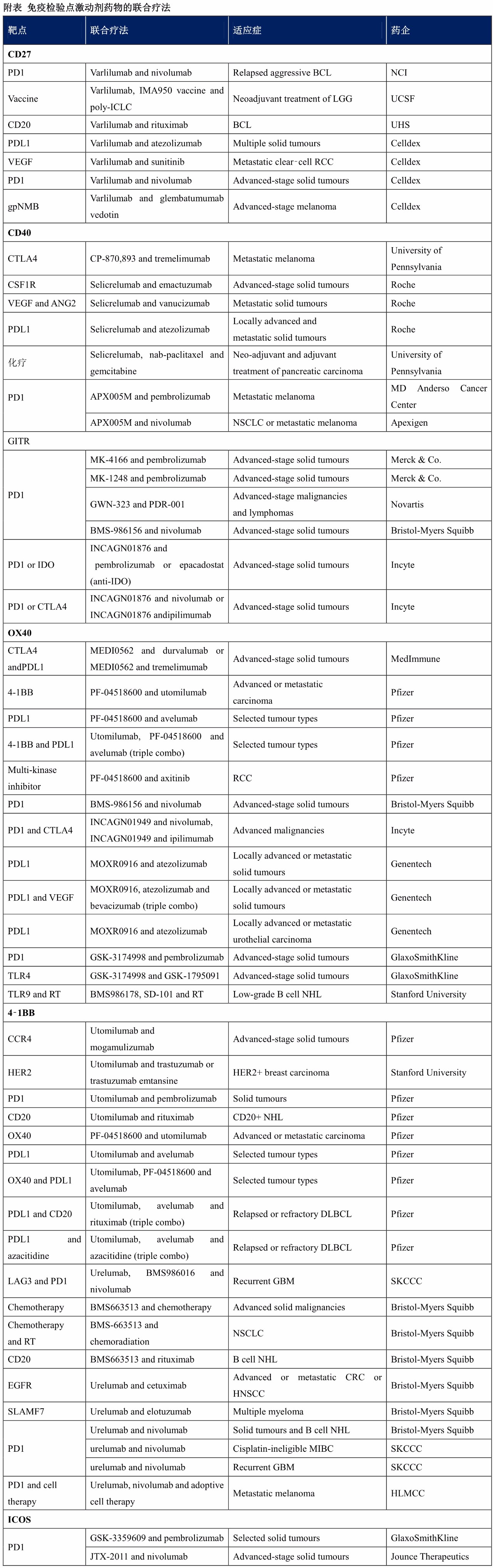
目前为止,免疫检验点激动剂抗体仍处于临床开发前期,仍需要数据积累。另外,很多免疫检验点激动剂抗体均作为与免疫检验点抑制剂抗体的联合疗法进行临床开发。
国内方面,目前已经申报临床的免疫检验点激动剂抗体包括信达生物的OX40抗体IBI-101和天演药业的4-1BB抗体ADG106。天演药业的动态精准抗体药物平台(DPL Platform)整合了计算生物学和生物技术,提高了对复杂抗原或独特表位获得功能抗体的能力。ADG-106已经相继获得美国、中国的临床批准,并与辉瑞、百时美施贵宝等的4-1BB抗体具有不同表位,“是目前唯一在非免疫缺陷小鼠的不同肿瘤模型中证明单一药效及与其他药物有协同作用的抗体,同时在高剂量水平下仍然显示出非常好的安全性”。
小编评论
目前来看,免疫检验点激动剂抗体有充分的发展空间。国内药企跟踪国际前沿的速度明显加快,除了信达生物、天演药业,相信有很多国内药企进入该领域。不同于免疫检验点抑制剂,激动剂抗体在抗体筛选、功能评价等方面都存在较大的技术难度。对于跟踪研发为主的国内新药研发环境来说,免疫检验点激动剂抗体有难度也意味着新的机会。
参考资料
The promise and challenges of immune agonist antibody development in cancer;