
随着默沙东帕博利珠单抗(2018/7/26)和百时美纳武单抗(2018/6/15)的相继获批,以及恒瑞、君实、信达等的相继提交其PD-1抗体的上市申请,国内PD-1的竞争已经入白热化阶段。
截止8月1日,国内已有34个PD-(L)1单抗获CDE受理(国内企业28个,国外企业6个,包括已上市的2个品种),根据临床试验登记平台显示,国内公开登记的PD-(L)1的临床试验已有133项,涉及14家国内企业的16个品种,6家国外企业的6个品种;从临床阶段看,III期临床56项,II期临床32项,I期临床35项,其他10项,III期临床占比达42%。
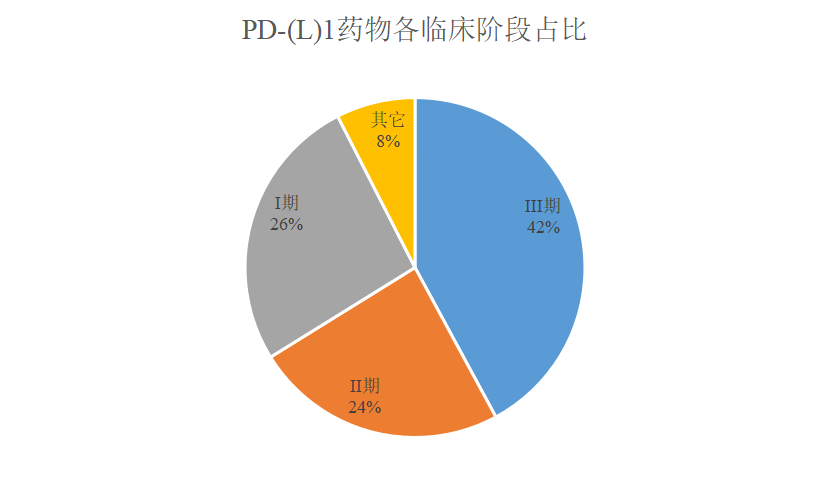
(1)各企业临床进度
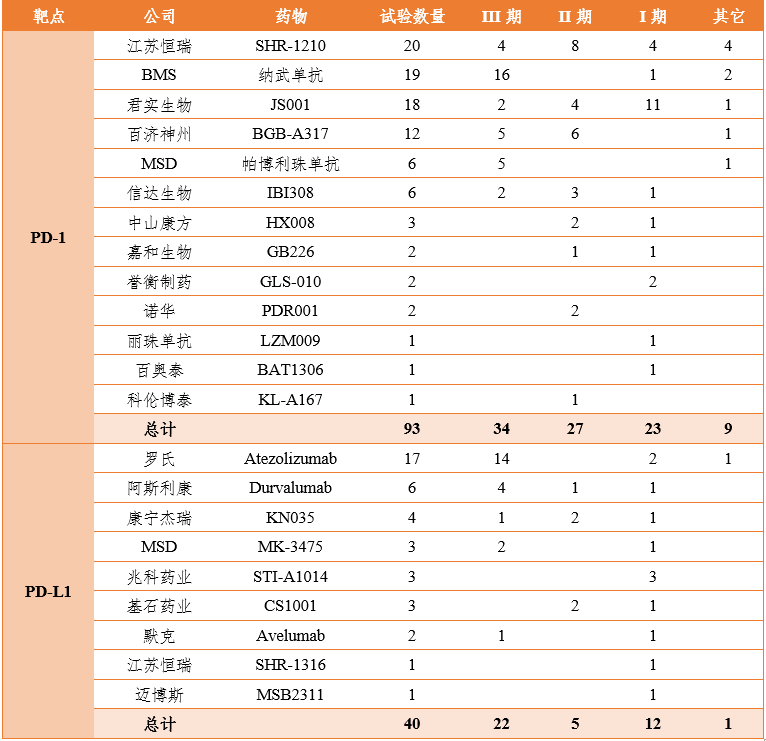
从生产企业角度来看,恒瑞医药、君实生物、信达生物、百济神州、康宁杰瑞5家企业已进展至III期临床,成为该领域的第一梯队;中山康方、嘉和生物,科伦博泰、基石药业均有品种处于II期临床。
值得注意的是,目前国内一些技术、资本雄厚的企业开始通过开发特色的PD-1/PD-L1抗体,走向全球市场,恒瑞医药的SHR-1316、康宁杰瑞/思路迪的KN035、百济神州的BGB-A317、复宏汉霖的HLX-10、丽珠单抗的LZM-009、君实生物的JS001和迈博斯的MSB2311等已先后向FDA递交新药临床试验。其中百济神州在国内分布开展了针对肝细胞癌(III期)、霍奇金淋巴瘤(II期)、膀胱尿路上皮癌(II期)、食管鳞状细胞癌(III期)、T细胞和NK细胞肿瘤(II期)等的6项国际多中心临床,而君实生物也有一项针对复发性或转移性鼻咽癌III期国际多中心临床正在开展中。
表 1 国内PD-(L)1抗体临床试验进展
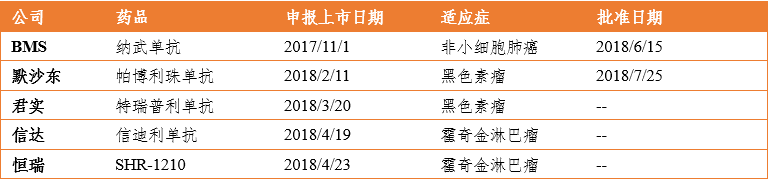
在第一梯队中,恒瑞、君实、信达均已提交上市申请。其中君实生物申请适应症为黑色素瘤,信达和恒瑞均为经典霍奇金淋巴瘤。值得注意的是信达和恒瑞提交的上市申请是基于单臂、二期的有条件批准上市。
表 2 国内已上市和提交上市申请的PD-1抗体
(2)适应症选择
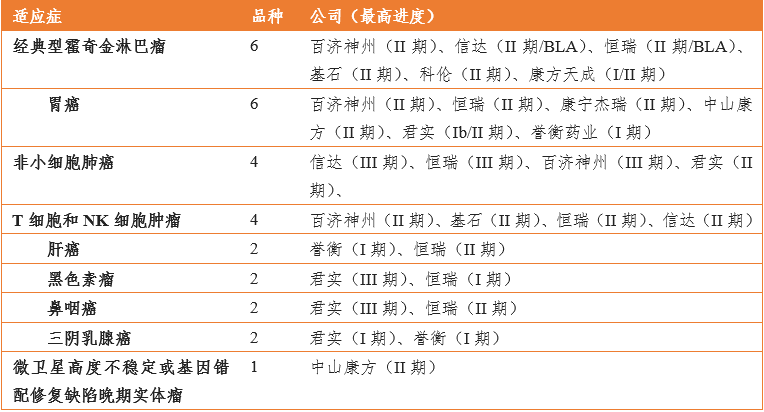
国内PD-(L)1单抗均以1类新药路径申报,目前有78项临床试验在不同的研究阶段,其适应症开发策略也不尽相同。
国内企业选择开发的适应症主要有霍奇金淋巴瘤(6家)、胃癌(6家)、非小细胞肺癌(4家)、T细胞和NK细胞肿瘤(4家),肝癌、黑色素瘤、鼻咽癌、三阴乳腺癌等。
表 3 国内PD-(L)1抗体主要适应症开发情况
根据已上市药物PD-(L)1抗体的临床表现情况,对于PD-(L)1表现高反应率的适应症类型包括:霍奇金淋巴瘤,促纤维增生性黑色素瘤,梅克尔细胞癌,微卫星高度不稳定的癌症,它们的反应率为50~90%。表现中等反应率的适应症类型包括:皮肤黑色素瘤,非小细胞肺癌,头颈癌,胃食管癌,尿路上皮癌,肾细胞癌,肝癌,宫颈癌和纵膈型大B细胞淋巴瘤。目前,恒瑞、信达均是以PD-1临床反应率较高的霍奇金淋巴瘤申请有条件批准上市,君实则为黑色素瘤。不过,国内企业研发上整体还是倾向于国内发病率比较多的癌种如胃癌、肝癌、肺癌等。不过有一些企业则独辟蹊径选择了市场存在强烈需求的适应症如三阴性乳腺癌,其市场空间还需依赖临床试验结果。
(3)联合治疗
临床上,免疫检查点抑制剂与其他药物联合用药可扩大适应症及解决单抗耐药。国内百济神州、江苏恒瑞、康宁杰瑞、君实生物、信达生物等在进行PD-(L)1的联合用药探索。国内PD-1联合用药不少是联合化疗和放疗,另有一些企业则选择与公司其他抗肿瘤产品进行联合布局。
百济神州在澳大利亚开展了2项联合用药临床,分别是PD-1/BTK抑制剂和PD-1/PARP抑制剂组合,恒瑞医药则大力推进PD-1抗体与其小分子抗癌新药阿帕替尼(商品名艾坦)的联合治疗,并力求攻克一些难治癌症,如小细胞肺癌。复宏汉霖HLX10(重组抗PD-1人源化单克隆抗体注射液)联合HLX04(重组抗VEGF人源化单克隆抗体注射液)用于晚期实体瘤临床试验注册获得国家药监局的审评受理。