
由苏州康宁杰瑞生物科技有限公司(康宁杰瑞)独立开发的重组HER2 双特异性抗体Fc融合蛋白注射液(KN026)于日前向中国国家食品药品监督管理总局递交临床申请,并获得受理,受理号CXSL1700095苏。
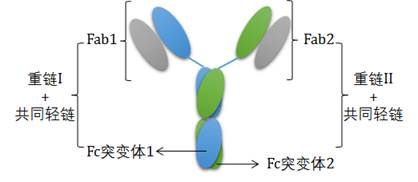
康宁杰瑞采用自主知识产权的Fc异二聚体平台技术和共同轻链开发了具有全球独立知识产权的双特异性抗体(KN026)。该抗体在完整保留Fc功能的同时,可有效识别两个不同的HER2表位。与罗氏的Herceptin + Perjeta联合用药相比,临床前药效研究显示KN026具有优效或等效的作用,对Her2低表达和Herceptin抗性肿瘤株也有抑制效果。KN026采用常规抗体生产工艺,产品得率、纯度和质量都达到Fc构架双特异性抗体的全球领先水平。
KN026项目是十三五重大新药创制专项课题,有望获得加速审批、在2018年进入临床试验。此外,公司计划在2017年完成KN026美国临床申报并随后启动临床试验。
在Her2阳性乳腺癌、胃癌等实体瘤中,Her2是主要驱动基因。KN026的研制成功将会为肿瘤患者提供新的有效治疗药物。
关于康宁杰瑞
苏州康宁杰瑞生物科技有限公司由徐霆博士2008年归国创建,在苏州设立研发中心6000余平方米,并成立博士后工作站。研发中先后投入3亿元人民币,建立了多个具有自主知识产权的生物制剂研发平台,包括多个抗体筛选平台、双特异抗体平台和混合抗体生产平台,并能够完成从抗体/蛋白药物早期筛选和工程化、成药性评价、细胞株构建和小试工艺、到中试放大及临床试验用药的生产及分析质控等全部流程。公司目前拥有多条cGMP生物大分子药物中试生产线和无菌制剂灌装车间。康宁杰瑞在研的生物大分子新药有十多个,已经申报临床批件9项,其中2项正在临床研究阶段(1项正在进行国际多中心开发)。康宁杰瑞位于江苏苏州的生产基地已启动筹建,力争在不久的将来为患者提供更多高效和优质的治疗药物, 解决国内药物可及性的同时积极参与国际竞争。
欲了解更多信息,请登录网站:www.alphamab.com